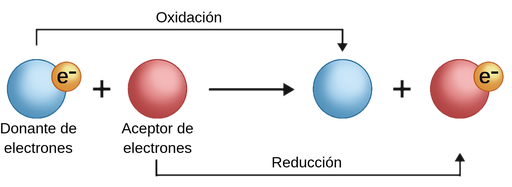
¿Qué son los procesos REDOX?
pérdida y ganancia de electrones
Pocos procesos son tan centrales como los de oxidación–reducción, también llamados REDOX. En este artí
culo veremos sus definiciones clásicas, algunos ejemplos sencillos y, sobre todo, por qué estos procesos son fundamentales en la vida, la energía y la tecnología.
En esencia, oxidar significa perder electrones y, al mismo tiempo, aumentar el número de oxidación. Por ejemplo:
Na(0) → Na(+1) + e-
El sodio metálico, que tiene número de oxidación 0, pierde un electrón y se convierte en ion sodio, con número de oxidación +1. Como ha perdido electrones, decimos que se oxida.
La reducción es el proceso complementario: una especie gana electrones y, al hacerlo, disminuye su número de oxidación. Un ejemplo clásico es:
e- + Cl(0) → Cl(-1)
El átomo de cloro, con número de oxidación 0, gana un electrón y se transforma en ion cloruro, con número de oxidación –1. En este caso, se ha reducido.
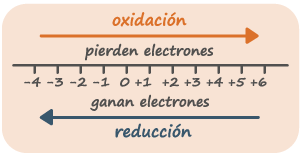
Podemos visualizarlo pensando en una escala de números de oxidación: cuanto más a la izquierda se mueve una especie (hacia valores más negativos), más reducida está; cuanto más a la derecha se desplaza (hacia valores positivos), más oxidada se encuentra. Lo importante es recordar que toda reacción redox implica siempre a dos partes: una que pierde electrones y otra que los gana.
Estas reacciones no son solo un tema teorico. Están presentes en la vida cotidiana y en la tecnología. En la respiración celular, nuestras células extraen energía a partir de cadenas de transporte electrónico. Las baterías y las pilas de combustible producen electricidad a través de reacciones redox cuidadosamente controladas. La corrosión de un metal, como el hierro que se oxida al contacto con el agua y el oxígeno, también es un proceso redox. Incluso en la industria, desde el blanqueo hasta la obtención de metales o la síntesis química, estos fenómenos tienen un rol central.
Un ejemplo rápido puede aclararlo aún más:
Fe(2+) + MnO4(-) → Fe(3+) + Mn(2+)
En esta reacción, el ion Fe²⁺ se transforma en Fe³⁺ al perder un electrón, por lo que se oxida. Mientras tanto, el MnO₄⁻ gana electrones y se convierte en Mn²⁺, lo que corresponde a una reducción. Para balancear correctamente estas reacciones se usa el método de las semirreacciones, asegurando que el número de electrones perdidos sea igual al de electrones ganados.
Al detenernos a pensar en estos procesos, surgen preguntas interesantes: ¿cómo medir la cantidad exacta de electrones transferidos? ¿qué ocurre en sistemas biológicos complejos como la fotosíntesis o la respiración celular? ¿y cómo podemos controlar la oxidación para evitar efectos no deseados como la corrosión?
La próxima vez que enciendas una batería, respires profundamente o veas una bicicleta oxidarse al sol, estarás presenciando la química redox en acción.
Principios de Quimica es una publicación apoyada por lectores. Para recibir nuevos posts y apoyar mi trabajo, considera convertirte en suscriptor de contenido gratis o suscriptor de pago.